第100回薬剤師国家試験
◆ 問91
分子間相互作用に関する記述のうち、正しいのはどれか。2つ選べ。-
酸素原子の電気陰性度は硫黄原子より大きいため、分子間に働く水素結合はH2Oの方がH2Sよりも強い。
-
静電的相互作用によるポテンシャルエネルギーは、距離の2乗に反比例する。
-
分散力は、ロンドン力とも呼ばれ、そのポテンシャルエネルギーは距離の4乗に反比例する。
-
ファンデルワールス相互作用は、分子間の距離により引力として働く場合と斥力として働く場合がある。
-
疎水性相互作用はファンデルワールス相互作用により説明される。
◆ 問91
◆領域・タグ
◆正解・解説
正解:1、4
酸素原子の電気陰性度は硫黄原子より大きいため、H2Oの水素原子は、H2Sの水素原子よりも強い正の電荷を帯びる。よって、分子間に働く水素結合はH2Oの方がH2Sよりも強い。
静電的相互作用によるポテンシャルエネルギーUは、距離に反比例する。なお、静電的相互作用によるポテンシャルエネルギーUは以下の式で表される。
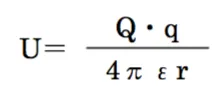
Q、q:粒子のもつ電荷、ε:溶媒の誘電率、r:粒子間の距離
分散力は、ロンドン力とも呼ばれ、そのポテンシャルエネルギーは距離の6乗に反比例する。
ファンデルワールス相互作用とは、電荷のない中性分子又は原子間に働く引力又は斥力のことであり、分子間の距離により引力として働く場合と斥力として働く場合がある。
疎水性相互作用とは、水中に存在する無機性物質(疎水物質)が水を避けて会合する際にみられる相互作用のことであり、水のエントロピーの増大により説明される。






