第101回薬剤師国家試験
◆ 問98
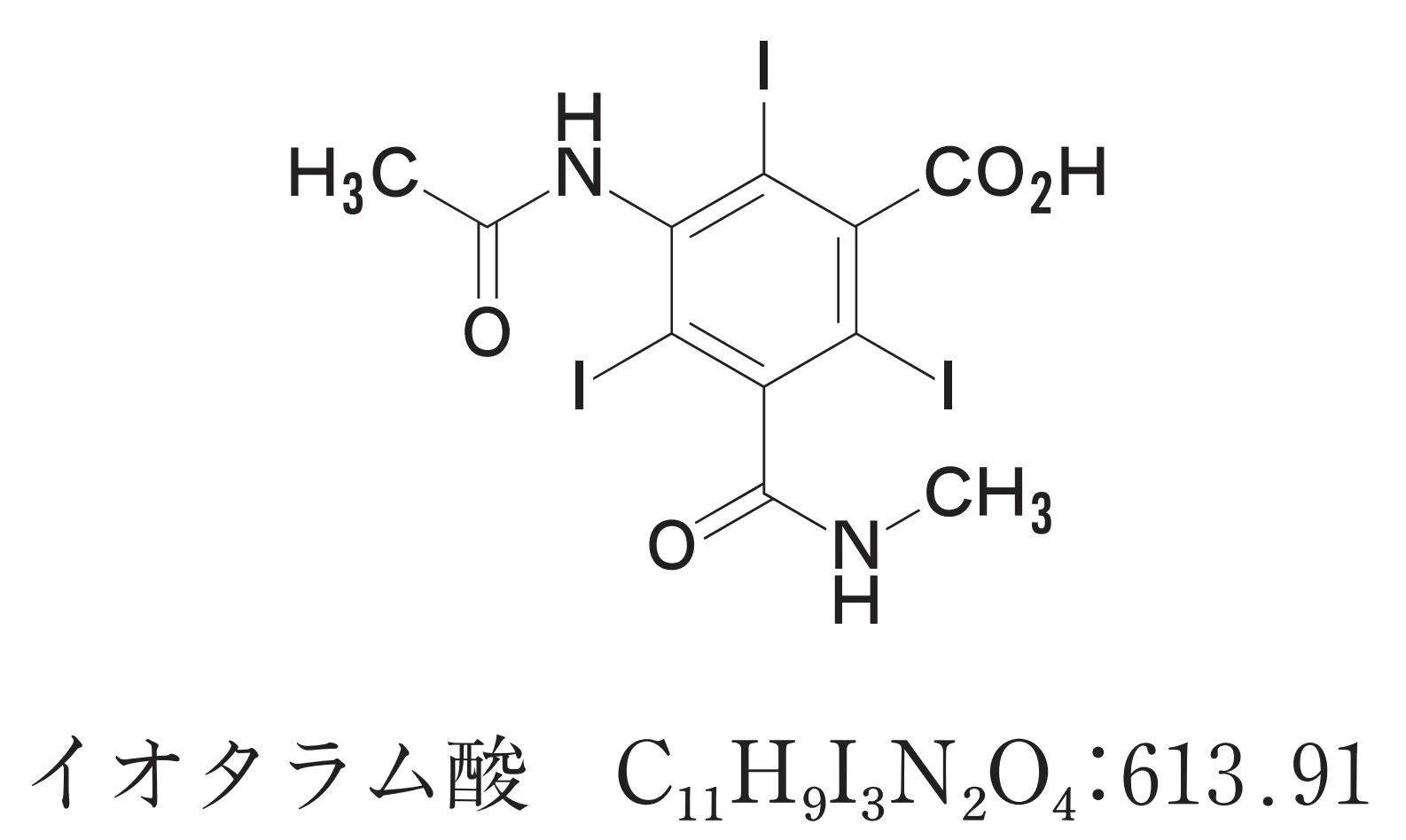
次の記述は日本薬局方イオタラム酸の定量法に関するものである。「本品を乾燥し、その約0.4 gを精密に量り、けん化フラスコに入れ、水酸化ナトリウム試液40 mLに溶かし、亜鉛粉末1 gを加え、還流冷却器を付けて30分間煮沸し、冷後、ろ過する。フラスコ及びろ紙を水50 mLで洗い、洗液は先のろ液に合わせる。この液に酢酸(100)5 mLを加え、0.1 mol/L硝酸銀液で滴定する(指示薬:テトラブロモフェノールフタレインエチルエステル試液1 mL)。ただし、滴定の終点は沈殿の黄色が緑色に変わるときとする。」
本品0.4500 gをとり、上記の定量法に従って、0.1 mol/L硝酸銀液(f=1.000)で滴定したところ、18.00 mLを消費した。このときイオタラム酸の含量%に最も近い数値を1つ選べ。
-
75
-
81.9
-
88.8
-
95.5
-
99.5
◆ 問98
◆領域・タグ
◆正解・解説
正解:2
イオタラム酸の定量法に関する問題である。本定量法では、イオタラム酸を水酸化ナトリウムと亜鉛末を用いて分解し、I-を遊離させ、遊離したI-を硫酸銀で滴定する。
イオタラム酸からは3 molのI-が遊離し、遊離したI-と硝酸銀は1:1で反応するため、イオタラム酸1 molに対して硝酸銀3 molが反応する(対応数:3)。
対応数が3であることから、0.1 mol/L硝酸銀液1 mLに対するイオタラム酸の量(対応量)は以下のように求めることができる。
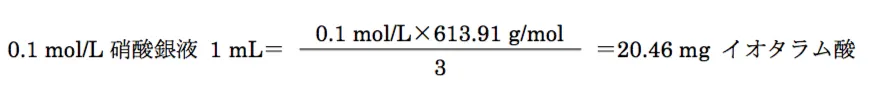
本設問の定量では、0.1 mol/L硝酸銀液(f=1.000)を18.00 mL消費していることから、本品に含まれるイオタラム酸の量を以下のように求めることができる。
イオタラム酸の量=20.46 mg/mL×18.00 mL×1.000=368.28 mg=0.368 g
本品の秤取量が0.4500 gであることから、含量(%)は以下のように求めることができる。
含量(%)=(0.368 g/0.4500 g)×100=81.77(%)






