第111回薬剤師国家試験
◆ 問178
ある非電解質薬物 25 mg を結晶又は非晶質固体分散体として、それぞれ一定温度の水 1.0 L に分散したところ、図に示す薬物濃度-時間曲線が得られた。この薬物の溶解に関する記述として、正しいのはどれか。2つ選べ。ただし、この薬物には結晶多形は存在しないものとする。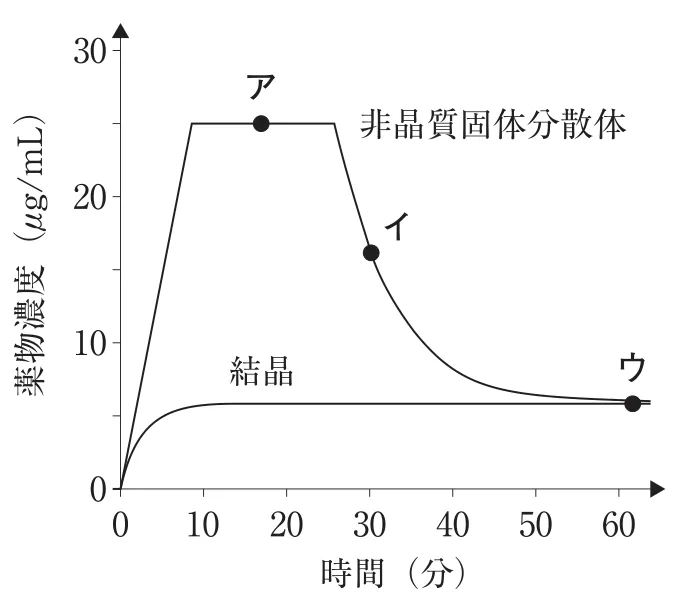
-
薬物結晶の飽和溶解度は約 25 μg/mL である。
-
アでは、薬物はすべて溶解しており、液は澄明である。
-
イでは、固相の薬物は一部非晶質として存在している。
-
イでは、液相の薬物は過飽和溶解している。
-
ウでは、薬物結晶が約5 mg 存在している。
◆ 問178
◆領域・タグ
◆正解・解説
正解:2、4
この問題の核心は、グラフ上の3つの点(ア、イ、ウ)がそれぞれどのような物理的状態にあるかを正確に読み取れるかにあります。特に、一時的に溶解度以上の濃度になる「過飽和現象」と、最終的に安定な「結晶」の飽和溶解度へ収束していく流れを理解することが重要です。
まず、グラフから読み取れる数値を整理しましょう。
・点ア(ピーク): 約 25 μg/mL
・点イ(中間): 約 15 μg/mL
・点ウ(最終): 約 5 μg/mL
・全投与量: 25 mg / 1.0 L = 25 μg/mL
「薬物結晶の飽和溶解度は約 25 μg/mL である」は、誤りです。・点イ(中間): 約 15 μg/mL
・点ウ(最終): 約 5 μg/mL
・全投与量: 25 mg / 1.0 L = 25 μg/mL
グラフの終着点である点ウ(約 5 μg/mL)が、熱力学的に安定な結晶状態における飽和溶解度を示しています。25 μg/mL という値は、非晶質として全量が一時的に溶け出している状態(点ア)の濃度です。
「アでは薬物はすべて溶解しており、液は澄明である」は、正しい記述です。
計算した通り、全投与量(25 mg)を 1.0 L に溶かした時の濃度は 25 μg/mL です。点アはこの数値と一致しているため、投与されたすべての薬物が溶液中に溶け込んでおり、不溶性の固体が存在しない「澄明な状態」であると言えます。
「イでは固相の薬物は一部非晶質として存在している」は、誤りです。
点アから点イへと濃度が低下していく過程は、過飽和溶液から薬物が「析出」している状態です。析出する際には、よりエネルギーが低く安定な構造である「結晶」として出てくるのが一般的です。一度溶けた非晶質が、不安定な非晶質のまま再び固形として存在することは考えにくいです。
「イでは液相の薬物は過飽和溶解している」は、正しい記述です。
結晶の本来の飽和溶解度は点ウ(約 5 μg/mL)です。点イの濃度(約 15 μg/mL)は、この飽和溶解度を大幅に上回っているため、「過飽和状態」にあると言えます。非晶質を利用することで、本来の溶解度以上の濃度を一時的に維持できるのがこの製剤のメリットです。
「ウでは薬物結晶が約 5 mg 存在している」は、誤りです。
点ウの濃度は約 5 μg/mL です。1.0 L の溶液中には、5 μg/mL × 1,000 mL = 5 mg の薬物が「溶解」しています。全投与量は 25 mg ですので、底に沈んでいる「結晶(固相)」の量は、25 mg − 5 mg = 20 mg となります。5 mg というのは「溶けている量」のことであり、存在している結晶の量ではありません。
【試験対策のポイント:非晶質(アモルファス)の性質】
非晶質は結晶に比べて分子の並びがバラバラでエネルギーが高いため、以下の特徴があります。
- メリット: 結晶よりも溶けやすく、一時的に高い濃度(過飽和)を作れるため、吸収性が向上します。
- デメリット: 熱力学的に不安定なため、時間が経つと安定な「結晶」へと変化(転移)し、溶解度が低下してしまいます。






