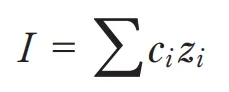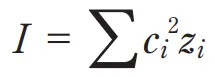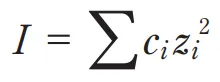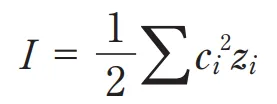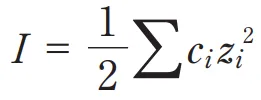第111回薬剤師国家試験
◆ 問2
イオン強度 I を求める式として正しいのはどれか。1つ選べ。ただし、ci はイオン種 i のモル濃度、zi はそのイオンの電荷である。◆ 問2
◆領域・タグ
◆正解・解説
正解:5
イオン強度 I の定義式は、
I = 1/2Σi ci zi2
である。各イオン種のモル濃度 ci に、電荷 zi の2乗を掛けた値を全イオン種にわたって合計し、最後に 1/2 を乗じる点がポイント。電荷を2乗するため、1価イオンより2価・3価イオンが不均衡に大きくイオン強度に寄与する(2価なら4倍、3価なら9倍)。
イオン強度は溶液中のイオン間の静電的相互作用の強さを表す指標であり、デバイ–ヒュッケルの理論においてイオンの活量係数 γ を求める基本量となる。活量係数は log γ ∝ -√(I) に比例して低下するため、イオン強度が高いほど実効的な濃度(活量)は理想溶液からずれる。
製剤設計(注射剤の等張化・緩衝液の調製)や薬物の溶解度・安定性の評価において重要な概念であり、式の形(½・Σ・c・z²)をそのまま覚えておきたい。