第111回薬剤師国家試験
◆問240-241
7月中旬に学校薬剤師が担当中学校の屋外プールの水質検査を実施した。採水時刻は午前11時、天候は晴れ、気温 29.5 ℃、水温 32 ℃であった。循環ろ過装置の運転は1 日当たり2 循環であり、消毒剤として塩素化イソシアヌル酸が自動注入されている。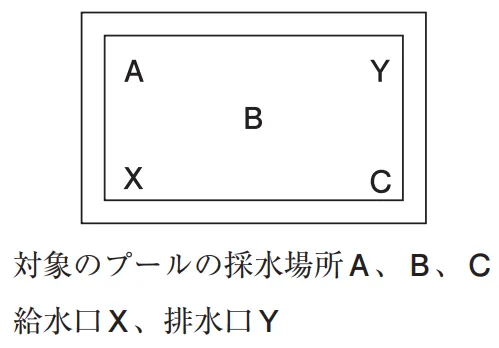
上図のプール3 ケ所(A~C)で遊離残留塩素を測定したところ、全て 0.4 mg/Lであった。その他の検査結果は次のとおりだった。
(検査結果)
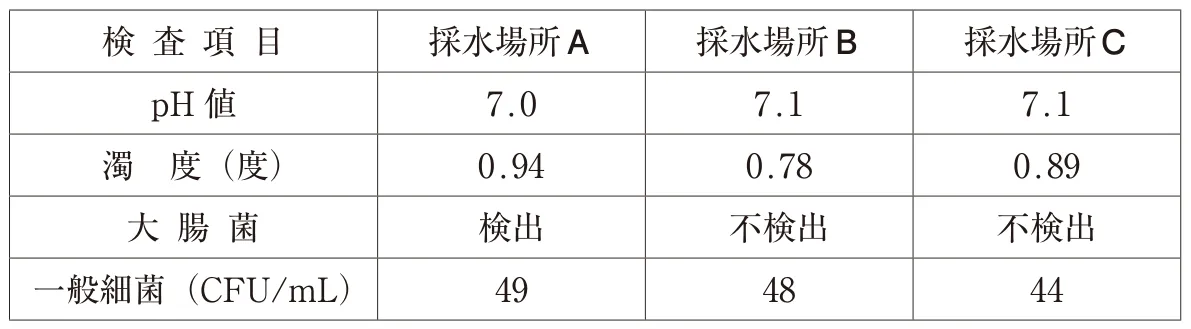
◆ 問240
Aから採取した水の過マンガン酸カリウム消費量を薬剤師が測定することにした。検水 100 mL をとり、これに過マンガン酸カリウム処理硫酸溶液5 mL を加え、さらに 0.002 mol/L 過マンガン酸カリウム溶液 10 mL を正確に加えた。5 分間煮沸した後、直ちに 0.005 mol/L シュウ酸ナトリウム溶液 10 mL を正確に加えて脱色させ、さらに 0.002 mol/L 過マンガン酸カリウム溶液で微紅色が消えずに残るまで滴定したところ、5.0 mL を要した。このとき、過マンガン酸カリウム消費量(mg/L)に最も近い値はどれか。1つ選べ。ただし、過マンガン酸カリウム溶液とシュウ酸ナトリウム溶液のファクターを 1.000、過マンガン酸カリウムの式量を 158 とする。-
8.0
-
12
-
16
-
80
-
160
◆ 問241
◆ 問240
◆領域・タグ
◆正解・解説
正解:3
この問題は、プール水に含まれる有機物の量を推定する指標となる「過マンガン酸カリウム消費量」を、逆滴定のデータから算出するものです。計算の手順を一つずつ丁寧に進めていきましょう。
1. 反応に使用した各試薬の物質量(mmol)を求めます
まず、実験で加えた各溶液に含まれる試薬の物質量を算出します。
- 最初に加えたKMnO4:0.002 mol/L × 10 mL = 0.020 mmol
- 過剰分を消去するために加えたNa2C2O4:0.005 mol/L × 10 mL = 0.050 mmol
- 逆滴定(残ったNa2C2O4の測定)に要したKMnO4:0.002 mol/L × 5.0 mL = 0.010 mmol
酸性条件下でのKMnO4とNa2C2O4の反応係数比は 2:5 です。逆滴定で消費されたKMnO4(0.010 mmol)と反応したNa2C2O4の量を計算します。
0.010 mmol × (5 / 2) = 0.025 mmol
これが、検水との反応後に溶液中に残っていたシュウ酸ナトリウムの量になります。3. 検水との反応で消費されずに残った過マンガン酸カリウム(過剰分)を求めます
加えたシュウ酸ナトリウム(0.050 mmol)のうち、逆滴定に回されなかった分(0.050 - 0.025 = 0.025 mmol)が、検水との反応で残っていた過マンガン酸カリウム(過剰分)を消去するために消費されました。
このシュウ酸ナトリウム(0.025 mmol)と反応したKMnO4の量は以下の通りです。
0.025 mmol × (2 / 5) = 0.010 mmol
4. 検水が消費した過マンガン酸カリウムの量を求めます最初に加えた量から、上記で求めた「検水との反応で消費されずに残った量(過剰分)」を差し引きます。
0.020 mmol(最初) - 0.010 mmol(残った量) = 0.010 mmol
これが、100 mLの検水に含まれる有機物の酸化に費やされたKMnO4の物質量となります。5. 単位を質量(mg/L)に換算します
KMnO4の式量は158ですので、まず検水100 mLあたりの質量を求めます。
0.010 mmol × 158 mg/mmol = 1.58 mg
これを1 L(1,000 mL)あたりの値にするため、10倍します。1.58 mg × 10 = 15.8 mg/L ≒ 16 mg/L
正解:3(16 mg/L)【試験対策のポイント:逆滴定の流れの把握】
過マンガン酸カリウム消費量の計算では、逆滴定のプロセスを混同しないことが重要です。「最初に加えたKMnO4」から「検水と反応せずに残ったKMnO4」を引くことで、目的の値を導き出すことができます。また、KMnO4とNa2C2O4の反応比「2:5」や、検水の量(今回は100 mL)に応じた最終的な換算を忘れないようにしましょう。
◆ 問241
◆領域・タグ
◆正解・解説
正解:4、5
この問題は、水質検査の結果(過マンガン酸カリウム消費量や細菌検査)からプールの汚染状況を正しく読み取り、適切な改善策を提案できるかを問う内容です。過マンガン酸カリウム消費量は、水中の有機物量の指標となります。
正解:4(入泳者数が多いことや、入泳前のシャワーが不十分であることが、過マンガン酸カリウム消費量に影響した可能性があることを助言する)
過マンガン酸カリウム消費量が増加する主な原因は、水中の有機物が増えることです。プールにおいて、人の汗、尿、皮脂、汚れなどは主要な有機物負荷となります。そのため、入泳者が多すぎることや、入る前の洗浄(シャワー)が不十分であると、これらの有機物が水中に持ち込まれ、消費量の数値を押し上げる原因となります。教員への助言として非常に適切です。
正解:5(大腸菌が検出された場合は、遊泳を一時中止し、消毒の強化や水の入れ替えなどの対策を講じるよう助言する)
大腸菌の検出は、糞便汚染の可能性を示唆しており、学校環境衛生基準においても「検出されないこと」と定められています。基準に適合しない場合は、利用者の健康被害を防ぐために、直ちに遊泳を中止させなければなりません。その後、原因の究明、塩素消毒の強化、補水・換水を行い、再検査で安全が確認されるまで使用を控えるよう助言するのが正しい対応です。
誤り:1
過マンガン酸カリウム消費量が多い(=有機物が多い)状態では、消毒のために加えられた塩素が有機物と反応し、発がん性が懸念される「トリハロメタン」などの副生成物が発生しやすくなります。抑制されるのではなく、むしろ生成を促進してしまうため、誤りです。
誤り:2
プールの「オーバーフロー(溢水)」は、汚れが溜まりやすい水面付近の水を排出し、水質を浄化する上で有効な手段です。オーバーフローを「させないように」補水することは、汚染物質をプール内に留めることにつながるため、不適切な助言となります。
誤り:3
循環ろ過装置の主な役割は、水中の砂、ゴミ、髪の毛などの「懸濁物(濁度成分)」を取り除くことです。水に溶け込んでいる有機物(溶存有機物)そのものを大幅に除去する能力は限定的であるため、過マンガン酸カリウム消費量を下げるための「主目的」とする説明としては不十分です。
【実務に役立つポイント:学校プールの水質基準】
学校環境衛生基準における主要な項目を整理しておきましょう。
学校環境衛生基準における主要な項目を整理しておきましょう。
- 遊離残留塩素: 0.4 mg/L 以上(1.0 mg/L 以下が望ましい)。
- pH値: 5.8 以上 8.6 以下。
- 過マンガン酸カリウム消費量: 12 mg/L 以下。
- 大腸菌: 検出されないこと。






