第111回薬剤師国家試験
◆問96-97
次の記述は、日本薬局方水酸化ナトリウムの定量に関するものである。この水酸化ナトリウム(NaOH:40.00)は不純物として炭酸ナトリウム(Na2CO3:105.99)のみを含むものとし、下線部イ及びエの時点をそれぞれ第一中和点、第二中和点とする。本品約1.5gを精密に量り、新たに煮沸して冷却した水40mLを加えて溶かし、15℃に冷却した後、フェノールフタレイン試液2滴を加え、ア0.5mol/L硫酸で滴定し、イ液の赤色が消えたときの0.5mol/L硫酸の量をウA(mL)とする。さらにこの液にメチルオレンジ試液2滴を加え、再び0.5mol/L硫酸で滴定し、エ液が持続する淡赤色を呈したときの0.5mol/L硫酸の量をB(mL)とする。(A-B)mLから水酸化ナトリウム(NaOH)の量を計算する。
0.5mol/L硫酸1mL=「 オ 」mgNaOH
◆ 問96
◆ 問97
前問の定量法において、本品 1.5000 g を量り、0.5 mol/L 硫酸( f = 1.000)で滴定したところ、B = 0.25 mL であった。本品中の不純物である炭酸ナトリウムの含量として最も近いのはどれか。1つ選べ。-
0.9%
-
1.8%
-
2.5%
-
3.6%
-
5.0%
◆ 問96
◆領域・タグ
◆正解・解説
正解:1、2
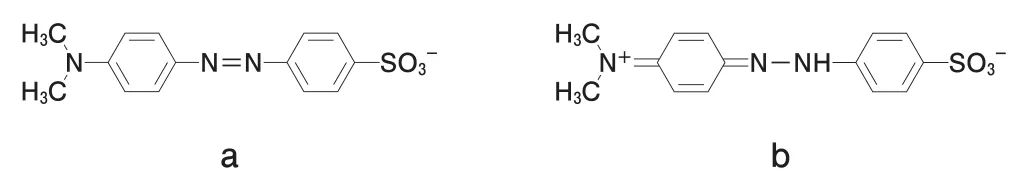
0.5 mol/L硫酸と0.5 mol/L塩酸の標定にはいずれも炭酸ナトリウムが標準試薬として用いられるため選択肢1は正しい。第一中和点のpHは本品量によらず一定であるため選択肢2も正しい。硫酸は2価の酸であるため塩酸に変えると滴定量は2倍になる(選択肢3は誤り)。メチルオレンジの変色はbからaへであり選択肢4の記述は逆。0.5 mol/L硫酸1 mLに対応するNaOHは40.00 mgであり80.00ではない(選択肢5は誤り)。
◆ 問97
◆領域・タグ
◆正解・解説
正解:2
B = 0.25 mLは第一中和点から第二中和点までの0.5 mol/L硫酸の滴定量で、NaHCO₃からH₂CO₃への反応に対応する。H₂SO₄は2価の酸であるため、H⁺のモル数は0.25 × 0.5 × 2 × 10⁻³ = 0.25 × 10⁻³ mol。Na₂CO₃も同モルなので0.25 × 10⁻³ mol。Na₂CO₃の質量は0.25 × 10⁻³ × 105.99 ≒ 26.5 × 10⁻³ g。含量は26.5 × 10⁻³/1.5000 × 100 ≒ 1.77%で、最も近いのは1.8%である。